热门搜索:分会介绍 | 会员名单 | 行业资讯

进口第一类医疗器械备案,备案人向国家食品药品监督管理总局提交备案资料。香港、澳门、台湾地区医疗器械的备案,参照进口医疗器械办理。办理备案的进口医疗器械,应当在备案人注册地或者生产地址所在国家(地区)获得医疗器械上市许可。备案人注册地或者生产地址所在国家(地区)未将该产品作为医疗器械管理的,备案人需提供相关证明文件,包括备案人注册地或者生产地址所在国家(地区)准许该产品合法上市销售的证明文件。
昨日,国家药监局发布2019年6月进口第一类医疗器械产品备案信息,共222个产品,其中涉及体外诊断产品45个。
小编也整理汇总前五个月的进口第一类医疗器械产品备案信息:
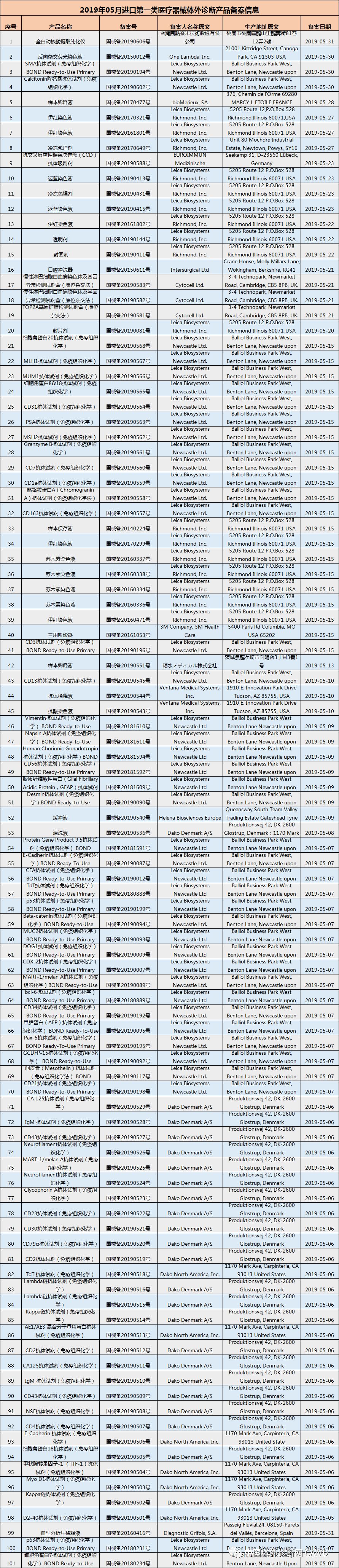
五月共225个产品,其中涉及体外诊断产品101个;
四月共237个产品,其中涉及体外诊断产品42个;
三月共172个产品,其中涉及体外诊断产品33个;
二月共204个产品,其中涉及体外诊断产品24个;
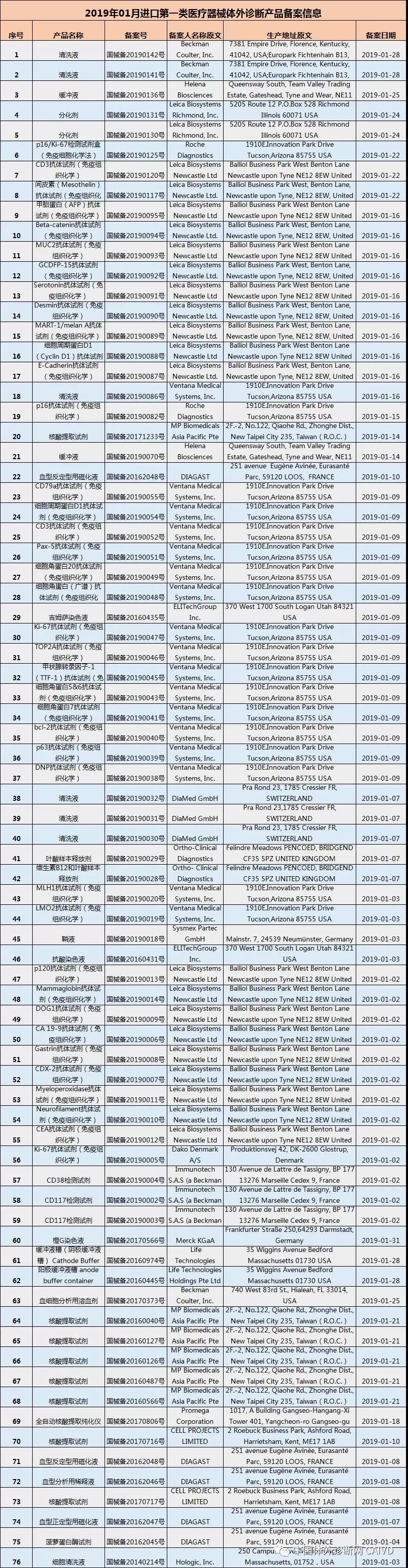
一月共545个产品,其中涉及体外诊断产品76个。
汇总如下:




邮政编码:200052 电话:021-63800152 传真:021-63800151 京ICP备15010734号-10 技术:网至普网站建设