
据CDE官网显示,日前,百利药业GNC-038四特异性抗体注射液的临床试验申请获得NMPA默示许可,用于复发或难治性非霍奇金淋巴瘤(R/R NHL)、复发或难治性急性淋巴细胞白血病(R/R ALL)和难治性/转移性实体瘤的治疗。

据百利药业官网显示,这也是目前全球首个获批临床的四特异性抗体。
百利药业成立于1996年,主要聚焦恶性肿瘤,研发有突破性疗效的创新抗体药物、抗体偶联药物(ADC),以及儿童药物、麻醉、重症、心血管急救药物等。GNC-038是其GNC(Guidance navigation and control,制导导航控制)平台下首个进入临床的候选药物,为四特异性结构的“靶向免疫”抗体,可同时靶向四个抗原,临床拟用于血液瘤和实体瘤的治疗。
具体而言,GNC-038是在IgG基础上串联3个scFv搭建成对称的四特异性抗体,其中,4-1BB、CD3可募集和激活T细胞,PD-L1可解除免疫逃逸,CD19可靶向肿瘤,这一PD-L1/4-1BB/CD3/CD19的组合可以看做在CD3/CD19双抗基础上,进一步辅以PD-L1阻断和4-1BB通路激活。
除GNC-038外,百利药业GNC平台现有多个候选药物处于申报、临床前及临床研究阶段。
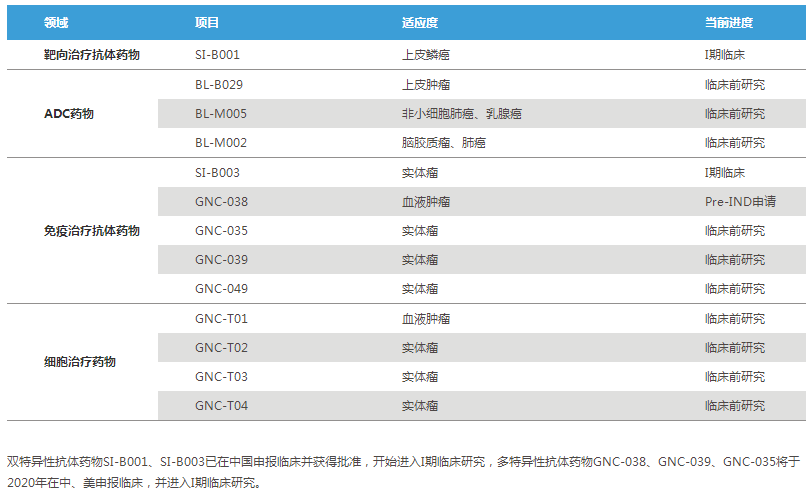
其中,SI-B001和SI-B003两款双抗已进入临床I期,SI-B001为EGFR/HER3双抗,用于局部晚期或转移性上皮肿瘤的治疗,包括食管鳞癌、肺鳞癌、三阴乳腺癌、头颈鳞癌、结直肠癌等;SI-B003靶点尚未披露,用于局部晚期、复发或转移性实体瘤的治疗,包括肾细胞癌、结直肠癌、黑色素瘤、非小细胞肺癌、尿路上皮癌等。
自PD-1/PD-L1等单克隆抗体引领肿瘤免疫疗法热潮以来,双特性抗体、三特异性抗体和多特异性抗体的研发也在不断涌现。
双特异性抗体方面,目前已经有3款上市,分别为:Fresenius的Removab、安进的Blincyto、罗氏的Hemlibra。根据去年《Nature Reviews Drug Discovery》发表的双抗综述,目前有上百个双抗药分子正在临床试验中被评估,预计未来几年将迎来全面爆发。
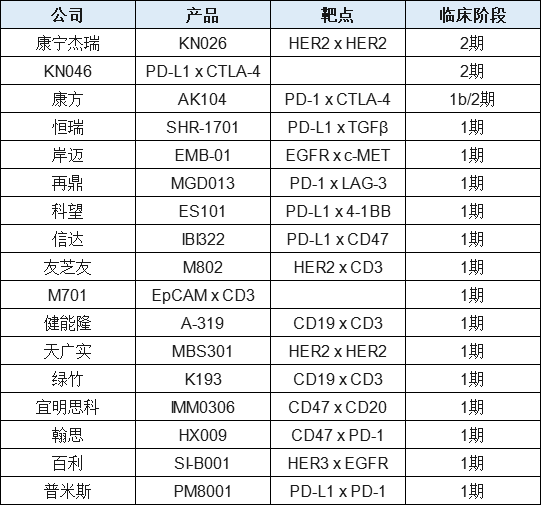
据相关统计,目前国内已有多家企业的双抗进入临床,从靶点来看,以PD-1/PD-L1、CTLA-4及HER2为靶点的项目居多,在BCMA、4-1BB、C-MET等靶点上也有所布局。
三特异性抗体方面,国外,赛诺菲的CD38/CD28/CD3三特异性抗体SAR442257于今年5月启动了临床研究,针对复发性难治性多发性骨髓瘤患者和非霍奇金淋巴瘤患者,计划入组57例患者,预计于2024年完成;罗氏则通过Contorsbody构建更紧凑的CD3三异性抗体,更利于T细胞与肿瘤细胞之间形成免疫突触;Dragonfly的TAA/CD16/NKG2D三特异性抗体TriNKET和Innate Pharma的TAA/CD16/NKp46三特异性抗体NKCE技术,则聚焦于NK细胞的肿瘤免疫。
国内,基石药业通过与Numab Therapeutics达成协议,获得PD-L1/4-1BB/HSA三特异性抗体ND021;泽璟制药与控股子公司Gensun Biopharma达成协议,获得三特异抗体ZGGS001;三生国健与Numab达成合作,开发和商业化一系列用于癌症治疗的新型多特异性抗体等。
邮政编码:200052 电话:021-63800152 传真:021-63800151 京ICP备15010734号-10 技术:网至普网站建设